Spermin
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
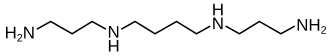
| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Spermin | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C10H26N4 | |||||||||||||||||||||
| Kurzbeschreibung |
hygroskopische Kristalle[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 202,34 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Siedepunkt |
141–142 °C (bei 66,5 Pa)[1] | |||||||||||||||||||||
| Löslichkeit |
leicht löslich in Wasser und Ethanol[1] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Spermin ist ein natürlich vorkommendes Polyamin, das unter anderem in menschlichem Sperma vorkommt und ihm seinen charakteristischen Geruch und Geschmack verleiht. Es ist als Polykation im zellulären Stoffwechsel aller Eukaryoten in verschiedenen Gewebetypen beteiligt (z. B. Blockade der Kaliumkanäle während der Initiationsphase des Aktionspotentials). Eine technische Verwendung ist möglich aufgrund seiner Eigenschaft, mit Stickstoffmonoxid (NO) wasserlösliche Komplexe zu bilden, wodurch das Gas leichter handhabbar wird. Es dient außerdem als Ausgangsstoff zur Synthese medizinisch interessanter Derivate.
Gewinnung
Ein Syntheseweg zum Spermin führt von Succinonitril durch Reduktion zu 1,4-Diaminobutan, anschließender Cyanoethylierung mit Acrylnitril zum Dicyanovorläufer und anschließender nochmaliger Reduktion.[3]
Biochemie
Spermin entsteht in Säugetierzellen durch Übertragung einer Aminopropylgruppe von decarboxyliertem S-Adenosylmethionin auf Spermidin, katalysiert durch Spermin-Synthase.[4] Sowohl Spermidin als auch Spermin konnten in Ribosomen, tRNA[5] und in Viren nachgewiesen werden. In wachsenden Zellen dient es zur Stabilisierung von räumlichen Strukturen von Ribonukleinsäuren und Proteinen.[6] Die Verringerung der Polyaminsynthese durch spezifische Hemmung der Ornithindecarboxylase führt zu einem Wachstumsstopp von Krebszellen und Tumoren.[7]
Forschungsgeschichte
1677 erwähnte Antoni van Leeuwenhoek erstmals das Vorkommen von Kristallen in Sperma und anderen Körperflüssigkeiten des Menschen.[8]
1870 isolierte Philipp Schreiner Spermin aus Sperma und wies nach, dass die bei Leukämie im Körper vorkommenden Charcotschen Kristalle das Phosphat dieser Base sind.[9] Das Ergebnis veröffentlichte er 1878 unter dem Titel Ueber eine neue organische Basis in thierischen Organismen in Justus Liebigs Annalen der Chemie.[10] Die Base wurde 1891 von Alexander Poehl aus Rinderhoden hergestellt.[9]
Die chemische Struktur des Spermins wurde zwischen 1923 und 1927 von Harold Dudley, Otto Rosenheim und F. Wrede aufgeklärt; in dieser Zeit gelang auch die Synthese.[11][12]
Verwendung
In der Kosmetik wird Spermin in Anti-Aging-Produkten zur Faltenreduktion zugesetzt.[13]
Siehe auch
Literatur
- Alexander Poehl: Die physiologisch-chemischen Grundlagen der Spermintheorie nebst klinischem Material zur therapeutischen Verwendung des Sperminum-Poehl. Hirschwald, Berlin 1896 (Digitalisat)
Einzelnachweise
- ↑ a b c d Eintrag zu Spermin. In: Römpp Online. Georg Thieme Verlag, abgerufen am 20. Juni 2014.
- ↑ a b Datenblatt Spermine bei Sigma-Aldrich, abgerufen am 17. Oktober 2016 (PDF).
- ↑ Harry P. Schultz: The Preparation of Spermine Tetrahydrochloride1 (1,12-Diamino-4,9-diazadodecane Tetrahydrochloride). In: J. Am. Chem. Soc. 70 (8), 1948, S. 2666–2667.
- ↑ Anthony E. Pegg: Introduction to the Thematic Minireview Series: Syxty plus years of polyamine research. In: Journal of Biological Chemistry. Band 293, Nr. 48, 2018, S. 18681–18692, doi:10.1074/jbc.TM118.006291 (englisch).
- ↑ L. Jovine, S. Djordjevic, D. Rhodes: The crystal structure of yeast phenylalanine tRNA at 2.0 angstrom resolution: Cleavage by Mg2+ in 15-year old crystals. In: Journal of Molecular Biology. 301, 2000, S. 401–414.
- ↑ J. Jänne et al.: Genetic approaches to the cellular functions of polyamines in mammals. In: FEBS (Hrsg.): European Journal of Biochemistry. Nr. 271, 2004, S. 877–894.
- ↑ F.L. Meyskens, E.W. Gerner: Development of Difluoromethylornithine (DFMO) as a Chemopreventive Agent. In: Clinical Cancer Research. Band 5, Mai 1999, S. 945–951.
- ↑ A. van Leeuwenhoek: Observationes D. Anthonii Leeuwenhoek, de natis e semine genitali animalculis. Letter dated November 1677. In: Philos. Trans. Roy. Soc. London. 12, 1678, S. 1040–1043.
- ↑ a b Mitteilung auf digitalis.uni-koeln.de, S. 387.
- ↑ Ph. Schreiner: Ueber eine neue organische Basis in thierischen Organismen. In: Justus Liebigs Annalen der Chemie. Band 194, Nr. 1, 1878, S. 68–84, doi:10.1002/jlac.18781940107.
- ↑ H. W. Dudley, O. Rosenheim, W. W. Starling: The chemical constitution of spermine. III. Structure and synthesis. In: Biochem. J. 20, 1926, S. 1082–1094. PMID 16743746.
- ↑ F. Wrede: Über die aus menschlichem Sperma isolierte Base Spermin. In: Dtsch. Med. Wochenschr. 51, 1925, S. 24.
- ↑ Patent WO2005013932: Use of Spermine and/or Spermidine against skin ageting in dietary, pharmaceutical or cosmetic compositions. Veröffentlicht am 30. Juli 2004, Erfinder: Fabio Rinaldi, Elisabetta Sorbellini, Sergio Baroni, Anna Benedusi.
