Stylopin
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
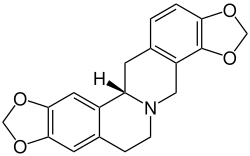
| |||||||||||||
| Natürliches (S)-Isomer | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Stylopin | ||||||||||||
| Andere Namen |
| ||||||||||||
| Summenformel | C19H17NO4 | ||||||||||||
| Kurzbeschreibung |
gelber Feststoff[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 323,3 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||
| Schmelzpunkt |
204 °C[1] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||
Stylopin ist eine organische Verbindung und ein Alkaloid. Es kommt in vielen Pflanzen vor und ist ein Intermediat in der Biosynthese vieler anderer Alkaloide.
Geschichte

Stylopin wurde erstmals 1902 aus der Pflanze Stylophorum diphyllum (Familie Mohngewächse) isoliert. Etwa dreißig Jahre später wurde die Verbindung auch aus dem hohlen Lerchensporn (Familie Erdrauchgewächse) isoliert und ihre Struktur aufgeklärt.[2]
Vorkommen und Biosynthese
Stylopin kommt insbesondere in den Pflanzenfamilien Erdrauchgewächse und Mohngewächse vor.[2] Es kommt beispielsweise neben Chelidonin im Schöllkraut vor.[3] Stylopin ist ein Intermediat in der Biosynthese diverser anderer Alkaloide in höheren Pflanzen. Dazu gehören Coptisin, Sanguinarin, Chelidonin, Macarpin,[S 3] Protopin und Rhoeadin. Selbst wird es aus Scoulerin gebildet. Dabei katalysieren zwei Cytochrom-P450-Enzyme die Bildung der Benzodioxoleinheiten. Im ersten Schritt entsteht so Cheilanthifolin,[S 4] im zweiten Stylopin.[4]
Herstellung
Stylopin kann in einer konvergenten Synthese hergestellt werden, die in ähnlicher Weise auch für die Herstellung verwandter Alkaloide angewandt wird. Die Synthese geht aus von 7,8-Dihydro-1,3-dioxolo[4,5-g]isochinolin,[S 5] das als Bortrifluorid-Komplex eingesetzt wird.[2]
Einzelnachweise
- ↑ a b c d e LGC Standards: Stylopine, (-)-(P) | CAS 84-39-9 | LGC Standards, abgerufen am 16. November 2024
- ↑ a b c Maria Chrzanowska: Synthesis of Isoquinoline Alkaloids. Total Synthesis of (±)-Stylopine. In: Journal of Natural Products. Band 58, Nr. 3, März 1995, S. 401–407, doi:10.1021/np50117a008.
- ↑ Alan R. Battersby, R. John Francis, Maurice Hirst, Edmundo A. Ruveda, James Staunton: Biosynthesis. Part XXI. Investigations on the biosynthesis of stylopine in Chelidonium majus. In: Journal of the Chemical Society, Perkin Transactions 1. Nr. 12, 1975, S. 1140, doi:10.1039/p19750001140.
- ↑ Wolfgang Bauer, Meinhart H. Zenk: Two methylenedioxy bridge forming cytochrome P-450 dependent enzymes are involved in (S)-stylopine biosynthesis. In: Phytochemistry. Band 30, Nr. 9, Januar 1991, S. 2953–2961, doi:10.1016/S0031-9422(00)98230-X.
Externe Links zu erwähnten Verbindungen
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu (S)-Stylopin: CAS-Nr.: 84-39-9, EG-Nr.: 884-572-4, ECHA-InfoCard: 100.361.001, PubChem: 440583, ChemSpider: 389482, Wikidata: Q27102969.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu (R)-Stylopin: CAS-Nr.: 2884-83-5, PubChem: 697545, ChemSpider: 607731, Wikidata: Q27280991.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Macarpin: CAS-Nr.: 23594-80-1, PubChem: 440929, ChemSpider: 389759, Wikidata: Q3841952.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Cheilanthifolin: CAS-Nr.: 483-44-3, PubChem: 101277425, Wikidata: Q105166168.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu 7,8-Dihydro-1,3-dioxolo(4,5-g)isochinolin: CAS-Nr.: 6882-28-6, EG-Nr.: 854-578-1, ECHA-InfoCard: 100.304.930, PubChem: 11344293, ChemSpider: 9519231, Wikidata: Q82287585.
