Sorafenib
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
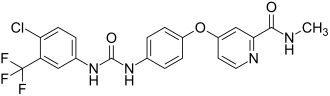
| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Sorafenib | |||||||||||||||||||||
| Andere Namen |
4-{4-[3-(4-Chlor-3-trifluormethylphenyl)ureido]phenoxy}pyridin-2-carbonsäuremethylamid (IUPAC) | |||||||||||||||||||||
| Summenformel | C21H16ClF3N4O3 | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
L01XE05 | |||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 464,83 g·mol−1 | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Sorafenib (Handelsname: Nexavar®, Hersteller: Bayer AG) ist ein Proteinkinaseinhibitor aus der Gruppe der Multi-Kinase-Inhibitoren. Er wird in Form von Tabletten angewendet und wirkt, indem es das Wachstum der Krebszellen verlangsamt und die Blutversorgung, die die Krebszellen wachsen lässt, unterbindet.
Anwendungsgebiete und Zulassung
Sorafenib zählt zu den Orphan-Arzneimitteln und ist seit 2006 für einige wenige Indikationen in der EU zugelassen. Diese waren zunächst nur die Behandlung des fortgeschrittenen Nierenkrebses, wenn eine Standardtherapie versagt hat oder ungeeignet ist, und die Behandlung von nicht mehr resezierbarem Leberzellkarzinom (hepatozelluläres Karzinom, HCC). Seit Juni 2014 ist Sorafenib in der EU zusätzlich zur Behandlung metastasierter differenzierter Schilddrüsenkarzinome, die nicht mehr auf eine Radiojodtherapie ansprechen, zugelassen.
Eine Phase-III-Studie zur Erstlinienbehandlung von fortgeschrittenem Hautkrebs war nicht erfolgreich und wurde vorzeitig abgebrochen.[2] Ebenso hat die klinische Phase-III-Studie (Indikation fortgeschrittener Lungenkrebs) den primären Endpunkt – eine Verlängerung des Gesamtüberlebens – nicht erreicht.[3]
Sorafenib wird spätestens seit der Bewertung der Expertengruppe Off-Label in Deutschland für die Erhaltungstherapie von Erwachsenen nach allogener Stammzelltransplantation bei akuter myeloischer Leukämie (AML) und bestehender FLT3-ITD-Mutation genutzt.[4][5]
Der Einsatz von Sorafenib nach allogener Stammzelltransplantation bei FLT3-Mutation fusst auf den Ergebnissen der SORMAIN-Studie.[6]
Pharmakologie
Als Multi-Kinase-Inhibitor hat Sorafenib mehrere Angriffspunkte:
- Es inhibiert die Raf-Kinase und blockiert somit die Raf-Signalkaskade. Es kommt zu einer verminderten Zellteilung und Proliferation.
- Es inhibiert mehrere Tyrosinkinasen; unter anderem die des VEGF-Signalweges. Es kommt zu einer Blockade der Signalkaskaden und zu einer reduzierten Tumor-Angiogenese.
Nebenwirkungen
Die häufigsten Nebenwirkungen sind Durchfall, Hautausschlag, Haarausfall, Hand-Fuß-Syndrom, verminderte Anzahl von Lymphozyten (Lymphopenie), Blutungen (Hämorrhagie), Bluthochdruck (arterielle Hypertonie), Übelkeit, Erbrechen, Hautrötung, Juckreiz, Müdigkeit (Erschöpfung), Schmerzen sowie erhöhte Amylase- und Lipasewerte.
Zwangslizenz
Das indische Patentamt hat dem Generikahersteller Natco Pharma eine Zwangslizenz zur Produktion von Sorafenib Tosylate für die nächsten acht Jahre zugesprochen – gegen die Zahlung einer Lizenzgebühr in Höhe von sechs Prozent der Verkaufserlöse.[7][8] Mit ein Auslöser für diese Entscheidung ist, dass Bayer die monatlichen Kosten für dieses Medikament mit annähernd 5.000 Euro beziffert. Mit diesem Patentübertrag kann der Generikahersteller die Kosten auf 175 US-Dollar senken, davon sind sechs Prozent an Bayer abzuführen. Dieses Urteil ist weltweit das erste, das einen Hersteller zwingt, seine Preise entweder selbst zu senken oder aber die Herstellung einem anderen Unternehmen zu überlassen. Bayer hat jedoch Widerspruch gegen die Zwangslizenzierung eingelegt.[9]
Zwangslizenzen sind im internationalen Handelsrecht verankert und werden in der Doha Declaration als zulässige Ausnahme zum TRIPS-Abkommen aufgelistet. Sie ermöglichen Staaten, bestehende Patente teilweise zu umgehen, um die öffentliche Gesundheit zu schützen – etwa wenn durch zu hohe Preise der Zugang von Patienten zu Medikamenten beeinträchtigt wird.
Literatur
Übersichtsartikel zur Pharmakologie
- D. Strumberg: Preclinical and clinical development of the oral multikinase inhibitor sorafenib in cancer treatment. In: Drugs Today. 41(12), 2005 Dec, S. 773–784. PMID 16474853.
- D. A. Murphy, S. Makonnen, W. Lassoued, M. D. Feldman, C. Carter, W. M. Lee: Inhibition of tumor endothelial ERK activation, angiogenesis, and tumor growth by sorafenib (BAY43-9006). In: Am J Pathol. 169(5), 2006 Nov, S. 1875–1885. PMID 17071608, PMC 1780219 (freier Volltext).
- Bewertung_Sorafenib_bei_Leukaemie
Übersichtsartikel zur Synthese und Analytik
- S. Afify, U. R. Rapp, P. Högger: Validation of a liquid chromatography assay for the quantification of the Raf kinase inhibitor BAY 43-9006 in small volumes of mouse serum. In: J Chromatogr B Analyt Technol Biomed Life Sci. 809(1), 2004 Sep 25, S. 99–103. PMID 15282098.
- D. Bankston, J. Dumas, R. Natero, B. Riedl, K. K. Monahan, R. Silbey: A scaleable synthesisof BAY 43-9006: apotent Raf kinase inhibitor for the treatment of cancer. In: Organic Process Research & Development. 6 (6), 2002, S. 777–781.
Weblinks
- Europäischer öffentlicher Beurteilungsbericht (EPAR) zu Nexavar ( vom 22. August 2006 im Internet Archive) der EMEA
Einzelnachweise
- ↑ a b Datenblatt Sorafenib bei Sigma-Aldrich, abgerufen am 3. Januar 2023 (PDF).
- ↑ Melanom: Studienabbruch wegen Wirkungslosigkeit von Sorafenib. ( vom 12. September 2013 im Internet Archive) In: Deutsches Ärzteblatt. 5. Dezember 2006.
- ↑ Nexavar® versagt bei Lungenkrebs. In: Deutsche Apotheker Zeitung. 22. Mai 2012.
- ↑ Sorafenib bei Leukämie - Bewertung. Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM), 2. Juli 2025, abgerufen am 18. Juli 2025.
- ↑ Sorafenib als Erhaltungstherapie nach allogener Stammzell-transplantation zur Behandlung von Erwachsenen mit akuter myeloischer Leukämie (AML) und einer FLT3-ITD-Mutation. Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM), 2. Juli 2025, abgerufen am 18. Juli 2025.
- ↑ Andreas Burchert, Gesine Bug, Lea V. Fritz, Jürgen Finke, Matthias Stelljes, Christoph Röllig, Ellen Wollmer, Ralph Wäsch, Martin Bornhäuser, Tobias Berg, Fabian Lang, Gerhard Ehninger, Hubert Serve, Robert Zeiser, Eva-Maria Wagner, Nicolaus Kröger, Christine Wolschke, Michael Schleuning, Katharina S. Götze, Christoph Schmid, Martina Crysandt, Eva Eßeling, Dominik Wolf, Ying Wang, Alexandra Böhm, Christian Thiede, Torsten Haferlach, Christian Michel, Wolfgang Bethge, Thomas Wündisch, Christian Brandts, Susanne Harnisch, Michael Wittenberg, Heinz-Gert Hoeffkes, Susanne Rospleszcz, Alexander Burchardt, Andreas Neubauer, Markus Brugger, Konstantin Strauch, Carmen Schade-Brittinger, Stephan K. Metzelder: Sorafenib Maintenance After Allogeneic Hematopoietic Stem Cell Transplantation for Acute Myeloid Leukemia With FLT3-Internal Tandem Duplication Mutation (SORMAIN). In: Journal of Clinical Oncology: Official Journal of the American Society of Clinical Oncology. Band 38, Nr. 26, 10. September 2020, S. 2993–3002, doi:10.1200/JCO.19.03345, PMID 32673171 (- PubMed).
- ↑ Erste Zwangslizenz für ein Medikament in Indien. auf: aerzte-ohne-grenzen.at, 12. März 2012.
- ↑ Urteil des indischen Patentamts (PDF; 2,2 MB) ( vom 21. März 2012 im Internet Archive)
- ↑ Bayer kämpft um Nexavar®-Patent. In: Deutsche Apotheker Zeitung. 7. Mai 2012.