Natriumhexafluoroarsenat
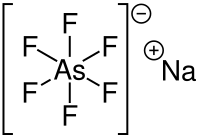
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||
| Allgemeines | ||||||||||
| Name | Natriumhexafluoroarsenat | |||||||||
| Summenformel | NaAsF6 | |||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 211,90 g·mol−1 | |||||||||
| Aggregatzustand |
fest[1] | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Toxikologische Daten | ||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||
Natriumhexafluoroarsenat ist eine anorganische Verbindung aus der Gruppe der Hexafluoroarsenate.
Eigenschaften und Verwendung
Natriumhexafluoroarsenat zeigt einen starken barokalorischen Effekt, also einen druckinduzierten Phasenübergang, der eine Temperaturänderung hervorruft, wodurch es sich möglicherweise für Kühlanwendungen eignet.[3] Natriumhexafluoroarsenat bildet mit Polyethylenoxid einen Polymerelektrolyten, der eine bessere Ionenleitfähigkeit aufweist als analoge Verbindungen mit Lithiumhexafluoroarsenat.[4] Daneben wird auch die Verwendung als Zusatz in Natriummetall-Batterien untersucht.[5]
Die Verbindung besitzt bei Raumtemperatur eine hexagonale Kristallstruktur mit der Raumgruppe R3 (Raumgruppen-Nr. 148).[6]
Einzelnachweise
- ↑ a b c d e Datenblatt Natriumhexafluorarsenat(V) bei Sigma-Aldrich, abgerufen am 14. Oktober 2024 (PDF).
- ↑ Nicht explizit in Verordnung (EG) Nr. 1272/2008 (CLP) gelistet, fällt aber mit der angegebenen Kennzeichnung unter den Gruppeneintrag Arsenverbindungen, mit Ausnahme der namentlich in diesem Anhang bezeichneten in der Datenbank ECHA CHEM der Europäischen Chemikalienagentur (ECHA), abgerufen am 3. März 2025. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Zhao Zhang, Takanori Hattori, Ruiqi Song, Dehong Yu, Richard Mole, Jie Chen, Lunhua He, Zhidong Zhang, Bing Li: Giant barocaloric effects in sodium hexafluorophosphate and hexafluoroarsenate. In: Journal of Applied Physics. Band 136, Nr. 3, 21. Juli 2024, doi:10.1063/5.0211085.
- ↑ Chuhong Zhang, Stephen Gamble, David Ainsworth, Alexandra M. Z. Slawin, Yuri G. Andreev, Peter G. Bruce: Alkali metal crystalline polymer electrolytes. In: Nature Materials. Band 8, Nr. 7, Juli 2009, S. 580–584, doi:10.1038/nmat2474.
- ↑ Shiyang Wang, Wenbin Cai, Zhihao Sun, Fanyang Huang, Yulin Jie, Yang Liu, Yawei Chen, Bo Peng, Ruiguo Cao, Genqiang Zhang, Shuhong Jiao: Stable cycling of Na metal anodes in a carbonate electrolyte. In: Chemical Communications. Band 55, Nr. 95, 2019, S. 14375–14378, doi:10.1039/C9CC07419H.
- ↑ Mamata Biswal, Monique Body, Christophe Legein, Gwenaël Corbel, Aymeric Sadoc, Florent Boucher: Structural Investigation of α- and β-Sodium Hexafluoroarsenate, NaAsF6, by variable Temperature X-ray Powder Diffraction and Multinuclear Solid-State NMR, and DFT Calculations. In: The Journal of Physical Chemistry C. Band 116, Nr. 21, 2012, S. 11682–11693, doi:10.1021/jp3040727.

