Magnesiumhydrogencarbonat
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
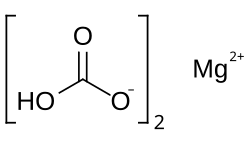
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Magnesiumhydrogencarbonat | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | Mg(HCO3)2 | ||||||||||||||||||
| Kurzbeschreibung |
Nur in wässriger Lösung beständiges Salz[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 146,33 g·mol−1 | ||||||||||||||||||
| Löslichkeit |
löslich in Wasser[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Magnesiumhydrogencarbonat ist ein nur in wässriger Lösung beständiges Salz. Es zählt zu den Härtebildnern des Wassers.[1]
Entstehung
Das Salz entsteht wenn Kohlensäurehaltiges Wasser mit Mineralien wie Magnesit oder Dolomit in Berührung kommt.[1]
Eigenschaften
Beim Erhitzen bzw. Eindunsten zerfällt es zu Magnesiumcarbonat, Kohlenstoffdioxid und Wasser:[1]
Einzelnachweise
- ↑ a b c d e Dr. Otto-Albrecht Neumüller: Römpps Chemie-Lexikon. 7. Auflage. Band 4. Franckh´sche Verlagshandlung, W. Keller & Co., Stuttgart 1974, ISBN 3-440-03854-8.
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.