Bis(hydroxylammonium)sulfat
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
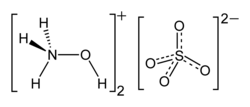
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Bis(hydroxylammonium)sulfat | |||||||||||||||
| Andere Namen |
Hydroxylammoniumsulfat | |||||||||||||||
| Summenformel | (NH3OH)2SO4 | |||||||||||||||
| Kurzbeschreibung |
farbloser bis weißer Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 164,14 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
1,88 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt |
> 120 °C (Zersetzung)[1] | |||||||||||||||
| Löslichkeit |
leicht in Wasser (587 g·l−1 bei 20 °C)[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Bis(hydroxylammonium)sulfat ist eine chemische Verbindung aus der Gruppe der Hydroxylammoniumsalze und Sulfate.
Gewinnung und Darstellung
Bis(hydroxylammonium)sulfat kann durch Säure-Base-Reaktion von Hydroxylamin mit Schwefelsäure gewonnen werden.
Eigenschaften
Bis(hydroxylammonium)sulfat ist ein farbloser bzw. weißer, wasserlöslicher und hygroskopischer Feststoff. Er ist bei erhöhter Temperatur instabil und seine wässrige Lösung reagiert sauer.[1] Der Feststoff zersetzt sich oberhalb von 150 °C stark exotherm mit einer Zersetzungswärme von −253,7 kJ·mol−1 bzw. −1546 kJ·kg−1.[4] Die Verbindung ist deflagrationsfähig. Hier wurde eine Deflagrationsgeschwindigkeit von 5,6 cm·min−1 und ein Druckanstieg bis 250 bar im geschlossenen System beobachtet.[5][6]
Verwendung
Bis(hydroxylammonium)sulfat wird als Reduktionsmittel in der Photographie und in der Färberei, Enthaarungsmittel für Häute und zur Reinigung von Aldehyden und Ketonen verwendet.[1]
Sicherheitshinweise
Bis(hydroxylammonium)sulfat ist ein explosionsgefährlicher Feststoff. Er reagiert bei Schlag oder Reibung, Erwärmung oder andere Zündquellen mit raschem Zerfall, wobei Schwefeloxide, Stickoxide, Hydroxylamin, Ammoniak und Stickstoff entstehen.[1]
In Deutschland ist Hydroxylammoniumsulfat entsprechend den Regelungen des Sprengstoffgesetzes als explosionsgefährlicher Stoff der Stoffgruppe C eingestuft.[7]
Weblinks
- International Chemical Safety Card 0898
- Patentanmeldung EP0945401A2: Verfahren zur Herstellung von Hydroxylammoniumsulfat. Angemeldet am 11. März 1999, veröffentlicht am 29. September 1999, Anmelder: Domo Caproleuna GmbH, Erfinder: Manfred Kretschmar, Norbert Leetsch.
Einzelnachweise
- ↑ a b c d e f g h i Eintrag zu Bis(hydroxylammonium)sulfat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 9. Januar 2019. (JavaScript erforderlich)
- ↑ Eintrag zu Bis(hydroxylammonium) sulphate in der Datenbank ECHA CHEM der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Toxikologische Bewertung von Hydroxylamin und seine Salze (PDF) bei der Berufsgenossenschaft Rohstoffe und chemische Industrie (BG RCI), abgerufen am 16. Oktober 2024.
- ↑ Jianna Wang; Hongyuan Wei; Lin Hao; Zhiqing Li; Da Wang: Thermal decomposition kinetic research on hydroxylamine inorganic salts and organic deriavatives in J. Therm. Anal. Calorim. 150 (2025) 9093–9104, doi:10.1007/s10973-025-14225-5.
- ↑ P.G. Urben; M.J. Pitt: Bretherick's Handbook of Reactive Chemical Hazards. 8. Edition, Vol. 1, Butterworth/Heinemann 2017, ISBN 978-0-08-100971-0, S. 1004.
- ↑ IChemE Symposium series no. 102: Pressure Hazards - Hazards from Pressure: Exothermic Reactions, Unstable Substances, Pressure Relief and Accidental Discharge, 1987, S102-01, Grewer, T.; Klais, O.: Pressure rise during homogeneous decomposition and deflagration.
- ↑ Bekanntmachung der gemäß § 2 SprengG von der BAM seit 1987 neu getroffenen Feststellungen pdf-Link.



