Cysteinsäure
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
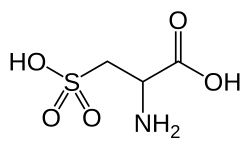
| |||||||||||||||||||
| Strukturformel ohne Stereochemie | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Cysteinsäure | ||||||||||||||||||
| Summenformel | C3H7NO5S | ||||||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 169,16 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Cysteinsäure, nach dem Anion auch als Cysteat bezeichnet, ist eine natürlich vorkommende nichtproteinogene Aminosäure. Es handelt sich um ein Oxidationsprodukt des Cysteins, bei dem die Thiolgruppe zu einer Sulfonsäuregruppe oxidiert ist.
Vorkommen
Cysteat tritt im Metabolismus diverser Mikroorganismen auf. Das Bakterium Paracoccus pantotrophus kann Cysteat durch Desaminierung zu 3-Sulfopyruvat, dann durch Reduktion in 3-Sulfolactat und dann Abspaltung von Hydrogensulfit zu Pyruvat umsetzen. Silicibacter pomeroyi bildet Cysteat durch Transaminierung: Dabei wird aus 3-Sulfolactat gebildetes 3-Sulfopyruvat mit Glutamat zu Cysteat und 2-Oxoglutarat umgesetzt. Dieses Bakterium kann Cysteat in einer einzelnen Reaktion zersetzen, wobei Ammonium, Hydrogensulfit und Pyruvat freigesetzt werden. Bestimmte Bakterien kommen mit Cysteinsäure beziehungsweise Cysteat als einzige Quelle von Kohlenstoff und Energie aus, dabei wird es insbesondere in Acetat umgewandelt. Cysteat ist auch als biosynthetischer Vorläufer von Sulfolipiden in Bakterien und Algen bekannt, beispielsweise von Capnin.[2]
Cysteat tritt auch als Intermediat der Biosynthese von Taurin in Mikroalgen auf. Diese geht von Sulfat und Serin aus. Letzteres wird zu 2-Aminoacrylat dehydratisiert, welches durch Phosphoadenosinphosphosulfat sulfatiert wird. Das so gebildete Cysteat wird im nächsten Schritt durch Decarboxylierung in Taurin umgewandelt.[3] Cysteat wurde auch als Intermediat der Biosynthese von Taurin in Säugetieren vermutet, was aber inzwischen widerlegt wurde. Der Biosyntheseweg dort verläuft stattdessen über Cysteinsulfinsäure und Hypotaurin, allerdings tritt Cysteat vermutlich als Abbauprodukt von Cysteinsulfinsäure auf.[2]
Herstellung
Cysteinsäure kann durch Oxidation von Cystein oder Cystin mit Perameisensäure gebildet werden. Dies eignet sich auch zur Quantifizierung von Cystein und Cystin in Proteinen, die selbst unter den für die Proteinhydrolyse nötigen Bedingungen nicht stabil sind.[4]
Eigenschaften
Das Monohydrat der Cysteinsäure kristallisiert im orthorhombischen Kristallsystem in der Raumgruppe P212121 (Raumgruppen-Nr. 19) mit den Gitterparametern a = 6,927 Å; b = 19,027 Å und c = 5,305 Å sowie 4 Formeleinheiten pro Elementarzelle.[5]
Weblinks
Einzelnachweise
- ↑ a b c d Eintrag zu L-Cysteic Acid bei TCI Europe, abgerufen am 26. August 2025.
- ↑ a b Alasdair M. Cook, Karin Denger, Theo H. M. Smits: Dissimilation of C3-sulfonates. In: Archives of Microbiology. Band 185, Nr. 2, März 2006, S. 83–90, doi:10.1007/s00203-005-0069-1.
- ↑ Rahul Tevatia, James Allen, Deepak Rudrappa, Derrick White, Thomas E. Clemente, Heriberto Cerutti, Yaşar Demirel, Paul Blum: The taurine biosynthetic pathway of microalgae. In: Algal Research. Band 9, Mai 2015, S. 21–26, doi:10.1016/j.algal.2015.02.012.
- ↑ E. Schram, S. Moore, E. J. Bigwood: Chromatographic determination of cystine as cysteic acid. In: Biochemical Journal. Band 57, Nr. 1, 1. Mai 1954, S. 33–37, doi:10.1042/bj0570033, PMID 13159945, PMC 1269701 (freier Volltext).
- ↑ W. A. Hendrickson, J. Karle: The crystal structure of L-cysteic acid monohydrate. In: Acta Crystallographica Section B Structural Crystallography and Crystal Chemistry. Band 27, Nr. 2, 15. Februar 1971, S. 427–431, doi:10.1107/S0567740871002322.