Blauzungenvirus
| Blauzungenvirus | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
Blauzungenvirus | ||||||||||||||||||||
| Systematik | ||||||||||||||||||||
| ||||||||||||||||||||
| Taxonomische Merkmale | ||||||||||||||||||||
| ||||||||||||||||||||
| Wissenschaftlicher Name | ||||||||||||||||||||
| Bluetongue virus | ||||||||||||||||||||
| Kurzbezeichnung | ||||||||||||||||||||
| BTV | ||||||||||||||||||||
| Links | ||||||||||||||||||||
|
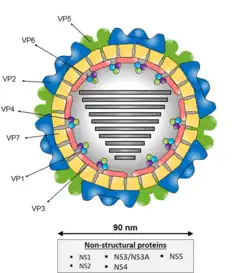
Das Blauzungenvirus (engl. Bluetongue virus, kurz BTV; Spezies Orbivirus caerulinguae) ist ein Virus aus der Familie Sedoreoviridae. Die Spezies ist die ehemalige Typusspezies der Gattung Orbivirus. BTV ruft bei Wiederkäuern die Blauzungenkrankheit hervor.
Die Viruspartikel von BTV sind unbehüllt und haben einem Durchmesser von 80 nm. Das Genom besteht aus linearer doppelsträngiger RNA (dsRNA), welche in zehn verschieden große Segmente unterteilt ist (multipartit). Vom BTV sind 24 verschiedene Serotypen mit typspezifischen Antigenen bekannt. Bei dem 2006 erstmals in Deutschland nachgewiesenen Virus handelte es sich seinerzeit um den Typ 8 (BTV-8). Die seit September 2023 und verstärkt seit Sommer 2024 in Europa – auch in Deutschland – sich ausbreitenden Variante ist BTV-3/NET2023.[3]
Das Virus wird durch Mücken aus der Gruppe Culicoides (Familie der Gnitzen) vom Frühjahr bis zum Herbst übertragen. Beim Saugen des Blutes eines infizierten Tieres nehmen sie das BTV-haltige Blut auf. Über ihren nun ebenfalls BTV-haltigen Speichel übertragen sie das Virus auf andere Tiere. Es erfolgt keine direkte Übertragung von Säugetier zu Säugetier.[4] Eine Temperatur von 25 bis 30 °C ist für die Virusvermehrung in den Gnitzen optimal. Im infizierten Tier bleibt das BTV etwa 40–80 Tage aktiv, kann danach aber noch längere Zeit (Schaf 100, Rind 240 Tage) mittels der Polymerase-Kettenreaktion (PCR) nachgewiesen werden.
Das Blauzungenvirus ist relativ fragil – die Infektiosität geht im leicht sauren Milieu verloren.[5]
Replikationszyklus
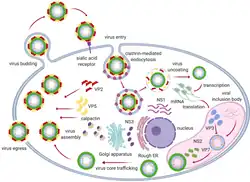

Die Virionen gelangen in die Wirtszelle durch die Bindung von des Kapsidproteins VP2 an Sialinsäur-Rezeptoren und entweder durch Clathrin-vermittelte Endozytose oder Makropinozytose. Der saure pH-Wert im Endosom bewirkt den Verlust von VP2 und bewirkt, dass die aus dem Kapsidprotein VP5 gebildete Membran durchlässig wird. Der Viruspartikel verliert so seine Kapsidschichten und der das Innere (mit demsegmentierten Genom) wird in das Zytoplasma der Wirtszelle freigesetzt. Die Transkription und Translation der Virus-Proteine findet unter Ausnutzung der Wirtszellmaschinerie statt. Im weiteren Verlauf werden die zusammengesetzten (assemblierten) Kernpartikel mit den Kapsidhüllen (Proteine VP5 und VP2) versehen, so dass reife Virionen entstehen. Die Partikel werden durch Knospung oder durch Lyse der Wirtszelle freigesetzt.[6]
Quellen
- ICTV: Species: Orbivirus caerulinguae Auf ictv.global
- Friedrich-Loeffler-Institut: Blauzungenkrankheit. Stand 13. Dezember 2018 [1].
- Polly Roy: Molecular Dissection of Bluetongue Virus. In: Thomas C. Mettenleiter, Francisco Sobrino (Hrsg.): Animal Viruses: Molecular Biology. Caister Academic Press, U.K., 2008; doi:10.21775/9781910190012, Kapitel 7 (englisch).
Einzelnachweise
- ↑ a b c d e ICTV: Bluetongue virus, EC 51, Berlin, Germany, July 2019; Email ratification March 2020 (MSL #35)
- ↑ ICTV Master Species List 2018b v1 MSL #34, Feb. 2019
- ↑ Virus in deutschen Viehbetrieben: Was man über die Blauzungenkrankheit wissen sollte. Auf: n-tv.de vom 24. August 2024.
- ↑ Blauzungenkrankheit Österreichische Agentur für Gesundheit und Ernährungssicherheit (AGES), 24. Juni 2025, abgerufen am 28. Juni 2025
- ↑ S. H. Hassan, C. Wirblich, M. Forzan, P. Roy: Expression and Functional Characterization of Bluetongue Virus VP5 Protein: Role in Cellular Permeabilization. In: Journal of Virology. Band 75, Nr. 18, September 2001, S. 8356, doi:10.1128/jvi.75.18.8356-8367.2001.
- ↑ a b Susan J. Dennis, Ann E. Meyers, Inga I. Hitzeroth, Edward P. Rybicki: African Horse Sickness: A Review of Current Understanding and Vaccine Development. In: MDPI: Viruses, Band 11, Nr. 9, Special Issue Equine Viruses, 11. September 2019, S. 844; doi:10.3390/v11090844 (englisch).