Bispinacolatodibor
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
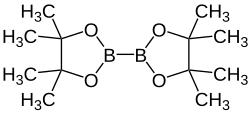
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Bispinacolatodibor | ||||||||||||||||||
| Andere Namen |
4,4,4′,4′,5,5,5′,5′-Octamethyl-2,2′-bi-1,3,2-dioxaborolan | ||||||||||||||||||
| Summenformel | C12H24B2O4 | ||||||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 253,94 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Bispinacolatodibor ist eine chemische Verbindung aus der Gruppe der Organoborverbindungen, die für diverse Reaktionen in der organischen Synthese verwendet wird.
Herstellung
Bispinacolatodibor kann ausgehend von Bortribromid hergestellt werden. Dieses wird zunächst mit Dimethylamin in Pentan zu Tris(dimethylamino)boran umgesetzt. Wird dieses wiederum mit Bortribromid in Pentan umgesetzt, wird Brombis(dimethylamino)boran erhalten. Dieses kann durch Reaktion mit elementarem Natrium zu Tetrakis(dimethylamino)dibor gekuppelt werden. Dieses kann durch Reaktion mit Pinacol unter Zugabe von Chlorwasserstoff in Diethylether zum Bispinacolatdibor umgesetzt werden.[2]
Reaktionen
Bispinacolatodibor kann zur Herstellung von entsprechenden Boronsäureestern dienen, das heißt solchen mit Pinacol als Alkoholkomponente. Alkine können unter Platinkatalyse doppelt boriert werden und ähnliche Reaktionen sind auch von Alkenen, Dienen, Allenen und Enonen bekannt. Arylhalogenide können unter Katalyse mit Palladium in Boronsäureester umgewandelt werden. Unter Katalyse mit Iridium oder Rhodium können auch Aromaten und Alkane boryliert werden.[3]
Alkene zweifach boryliert werden, wenn Bis(dibenzylidenaceton)platin(0) als Katalysator verwendet wird. Gute Resultate werden insbesondere bei Cycloalkenen mit einer gewissen Ringspannung erzielt, beispielsweise Cyclopenten oder Norbornen. Andere Verbindungen wie Cycloocten reagieren hingegen schlecht.[4] In Gegenwart von Tetrakis(triphenylphosphin)platin(0) als Katalysator können Allene mit Bispinacolatodibor doppelt boryliert werden.[5]
Durch Kreuzkupplung mit Bispinacolatodibor können Chloraromaten, Bromaromaten und aromatische Triflate zu Boronsäureestern umgesetzt werden. Als Katalysator dient Bis(dibenzylidenaceton)platin(0) mit Tricyclohexylphosphin.[6] Alkylbenzole können in Gegenwart einer katalytischen Menge Palladium auf Kohle in benzylischer Position boryliert werden.[7]
Bispinacolatodibor eignet sich außerdem als Reduktionsmittel für die Kupplung von Alkylbromiden beispielsweise 4-Brom-N-tosylpiperidin mit 1-Bromheptan. Als Katalysator dient dabei Nickel(II)-iodid mit einem cyclischen Aminliganden.[8]
Einzelnachweise
- ↑ a b c d e f Eintrag zu Bis(pinacolato)dibor, >99.0% bei TCI Europe, abgerufen am 8. Juni 2025.
- ↑ BIS(PINACOLATO)DIBORON. In: Organic Syntheses. Band 77, 2000, S. 176, doi:10.15227/orgsyn.077.0176.
- ↑ Xinyu Liu: Bis(pinacolato)diboron. In: Synlett. Nr. 15, 2003, S. 2442–2443, doi:10.1055/s-2003-43344.
- ↑ Tatsuo Ishiyama, Masafumi Yamamoto, Norio Miyaura: Diboration of alkenes with bis(pinacolato)diboron catalysed by a platinum(0) complex. In: Chemical Communications. Nr. 7, 1997, S. 689–690, doi:10.1039/a700878c.
- ↑ Tatsuo Ishiyama, Takahiro Kitano, Norio Miyaura: Platinum(0)-catalyzed diboration of allenes with bis(pinacolato)diboron. In: Tetrahedron Letters. Band 39, Nr. 16, April 1998, S. 2357–2360, doi:10.1016/S0040-4039(98)00199-3.
- ↑ Tatsuo Ishiyama, Kousaku Ishida, Norio Miyaura: Synthesis of pinacol arylboronates via cross-coupling reaction of bis(pinacolato)diboron with chloroarenes catalyzed by palladium(0)–tricyclohexylphosphine complexes. In: Tetrahedron. Band 57, Nr. 49, Dezember 2001, S. 9813–9816, doi:10.1016/S0040-4020(01)00998-X.
- ↑ Tatsuo Ishiyama, Kousaku Ishida, Jun Takagi, Norio Miyaura: Palladium-Catalyzed Benzylic C–H Borylation of Alkylbenzenes with Bis(pinacolato)diboron or Pinacolborane. In: Chemistry Letters. Band 30, Nr. 11, 1. November 2001, S. 1082–1083, doi:10.1246/cl.2001.1082.
- ↑ Hailiang Xu, Chenglong Zhao, Qun Qian, Wei Deng, Hegui Gong: Nickel-catalyzed cross-coupling of unactivated alkyl halides using bis(pinacolato)diboron as reductant. In: Chemical Science. Band 4, Nr. 10, 2013, S. 4022, doi:10.1039/c3sc51098k.
