Bariumchlorit
| Strukturformel | |||||||
|---|---|---|---|---|---|---|---|
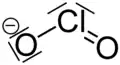
| |||||||
| Allgemeines | |||||||
| Name | Bariumchlorit | ||||||
| Summenformel | Ba(ClO2)2 | ||||||
| Externe Identifikatoren/Datenbanken | |||||||
| |||||||
| Eigenschaften | |||||||
| Molare Masse | 272,23 g·mol−1 | ||||||
| Aggregatzustand |
fest | ||||||
| Schmelzpunkt | |||||||
| Sicherheitshinweise | |||||||
| |||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||
Bariumchlorit ist eine chemische Verbindung aus der Gruppe der Chlorite.
Gewinnung und Darstellung
Im Labor gewinnt man es durch Reaktion von Chlordioxid mit Bariumhydroxid und Wasserstoffperoxid:[4]
Eigenschaften
Bariumchlorit ist ein Feststoff, welcher sich bei Erhitzung auf 190 °C explosionsartig zersetzt. Er kommt auch als Hydrat Ba(ClO2)2·3,5 H2O vor, welches eine monokline Kristallstruktur mit der Raumgruppe C2/c (Raumgruppen-Nr. 15) besitzt.[5]
Verwendung
Bariumchlorit kann zur Herstellung von Chloriger Säure oder Natriumchlorit verwendet werden.[6]
Einzelnachweise
- ↑ P. G. Urben: Bretherick's handbook of reactive chemical hazards. 2006, ISBN 0-12-372563-1 (Seite 96 in der Google-Buchsuche).
- ↑ Eintrag zu Bariumsalze in der GESTIS-Stoffdatenbank des IFA, abgerufen am 29. Dezember 2024. (JavaScript erforderlich)
- ↑ Nicht explizit in Verordnung (EG) Nr. 1272/2008 (CLP) gelistet, fällt aber mit der angegebenen Kennzeichnung unter den Gruppeneintrag barium salts, with the exception of barium sulphate, salts of 1-azo-2-hydroxynaphthalenyl aryl sulphonic acid, and of salts specified elsewhere in this Annex in der Datenbank ECHA CHEM der Europäischen Chemikalienagentur (ECHA), abgerufen am 29. Dezember 2024. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ G. Brauer (Hrsg.): Handbook of Preparative Inorganic Chemistry 2nd ed., vol. 1, Academic Press 1963, S. 312.
- ↑ Barium chlorite hydrate, Ba(ClO2)2·3.5H2O Acta Cryst. (2005). C61, i49-i50 doi:10.1107/S010827010500925X
- ↑ M. Mazumdar: Rudiments of Chemistry. 1. Auflage. 2006, ISBN 81-89781-53-7 (Seite 382 in der Google-Buchsuche).
