Arsen(III)-iodid
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
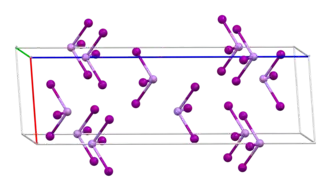
| ||||||||||||||||
| _ As3+ _ I− | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Arsen(III)-iodid | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Verhältnisformel | AsI3 | |||||||||||||||
| Kurzbeschreibung |
roter Feststoff mit stechendem Geruch[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 455,64 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Dichte |
4,38 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
403 °C[1] | |||||||||||||||
| Löslichkeit |
| |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||
| ΔHf0 |
−58,2 kJ/mol[4] | |||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Arsen(III)-iodid ist eine anorganische chemische Verbindung des Arsens aus der Gruppe der Iodide.
Gewinnung und Darstellung
Arsen(III)-iodid kann durch Reaktion von Arsen(III)-chlorid mit Kaliumiodid oder aus den Elementen gewonnen werden.[5]
Es kann auch aus Arsen(III)-oxid durch Reaktion mit Salzsäure und einer Kaliumiodid-Lösung gewonnen werden.[6]
Eigenschaften
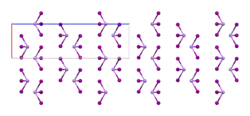
Arsen(III)-iodid ist ein rot-oranger Feststoff mit stechendem Geruch, der sich in Wasser langsam zersetzt.[1]
An Luft zersetzt er sich allmählich zu Iod und Arsen(III)-oxid. Er besitzt eine trigonale Kristallstruktur mit der Raumgruppe R3 (Raumgruppen-Nr. 148). Ab 110 °C liegt die Verbindung als Hochtemperaturmodifikation mit einer Kristallstruktur mit der Raumgruppe P3212 (Nr. 153) vor.[7]
Verwendung
Arsen(III)-iodid wurde früher zur Behandlung von Dermatitis bei Katzen und als Donovan’s Lösung zur Behandlung von Hautentzündungen und anderen Erkrankungen verwendet.[5]
Einzelnachweise
- ↑ a b c d e f g h i Eintrag zu Arsen(III)-iodid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 24. April 2016. (JavaScript erforderlich)
- ↑ Franz von Bruchhausen, Siegfried Ebel, Eberhard Hackenthal: Hagers Handbuch der Pharmazeutischen Praxis: Stoffe A-K. Springer DE, 1999, ISBN 978-3-642-58387-2, S. 107 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Nicht explizit in Verordnung (EG) Nr. 1272/2008 (CLP) gelistet, fällt aber mit der angegebenen Kennzeichnung unter den Gruppeneintrag Arsenverbindungen, mit Ausnahme der namentlich in diesem Anhang bezeichneten in der Datenbank ECHA CHEM der Europäischen Chemikalienagentur (ECHA), abgerufen am 3. März 2025. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-5.
- ↑ a b Eintrag zu ARSENIC TRIIODIDE in der Hazardous Substances Data Bank (via PubChem), abgerufen am 5. August 2013.
- ↑ Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 575.
- ↑ Jean D’Ans, Ellen Lax: Taschenbuch für Chemiker und Physiker. Springer DE, 1997, ISBN 3-540-60035-3, S. 306 (eingeschränkte Vorschau in der Google-Buchsuche).

