Americium(III)-chlorid
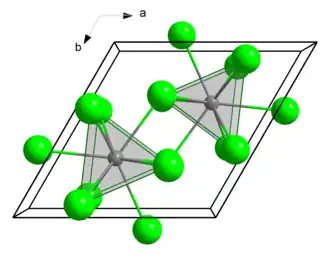
| Kristallstruktur | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||
| _ Am3+ _ Cl− | ||||||||||
| Kristallsystem | ||||||||||
| Raumgruppe |
P63/m (Nr. 176) | |||||||||
| Gitterparameter |
a = 738,2 pm | |||||||||
| Koordinationszahlen |
Am[9], Cl[3] | |||||||||
| Allgemeines | ||||||||||
| Name | Americium(III)-chlorid | |||||||||
| Andere Namen |
Americiumtrichlorid | |||||||||
| Verhältnisformel | AmCl3 | |||||||||
| Kurzbeschreibung |
rosafarbene hexagonale Kristalle[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 349,42 g·mol−1 | |||||||||
| Aggregatzustand |
fest | |||||||||
| Dichte |
5,87 g·cm−3[2] | |||||||||
| Schmelzpunkt | ||||||||||
| Siedepunkt |
1253 °C[3] | |||||||||
| Gefahren- und Sicherheitshinweise | ||||||||||
 Radioaktiv | ||||||||||
| ||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||
Americium(III)-chlorid ist ein Chlorid des künstlichen Elements und Actinoids Americium mit der Summenformel AmCl3. In diesem Salz tritt Americium in der Oxidationsstufe +3 auf.[5]
Eigenschaften
Americium(III)-chlorid bildet rosafarbene hexagonale Kristalle. Seine Kristallstruktur ist isotyp mit Uran(III)-chlorid. In der Struktur werden die Americiumatome von je neun Chloratomen umgeben, als Koordinationspolyeder ergibt sich dabei ein dreifach überkapptes, trigonales Prisma mit den Gitterparametern a = 738 pm und c = 421 pm und zwei Formeleinheiten pro Elementarzelle.[1] Der Schmelzpunkt der Verbindung liegt bei 715 °C.
Das Hexahydrat (AmCl3·6 H2O) weist eine monokline Kristallstruktur auf mit: a = 970,2 pm, b = 656,7 pm und c = 800,9 pm sowie β = 93° 37'; Raumgruppe: P2/n (Nr. 13, Stellung 2).[6]
Verwendung
Americium(III)-chlorid kann in einer NaCl-Salzschmelze in Gegenwart von Americium leichter zu Americium(II)-chlorid reduziert werden. Dies kann zur Trennung des Americiums von Plutonium genutzt werden.[7][8]
Einzelnachweise
- ↑ a b c Dale L. Perry: Handbook of Inorganic Compounds. CRC Press, 1995, ISBN 978-0-8493-8671-8, S. 15 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Americium(III)-chlorid bei www.webelements.com.
- ↑ F. Weigel, W. Schuster: The vapor pressure of americium(III) chloride: An ultramicro apparatus for the determination of saturation vapor pressures of actinide halides, in: Journal of the Less Common Metals, 1985, 113 (1), S. 157–176 (doi:10.1016/0022-5088(85)90157-2).
- ↑ Die von der Radioaktivität ausgehenden Gefahren gehören nicht zu den einzustufenden Eigenschaften nach der GHS-Kennzeichnung. In Bezug auf weitere Gefahren wurde dieser Stoff entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ L. B. Asprey, T. K. Keenan, F. H. Kruse: Crystal Structures of the Trifluorides, Trichlorides, Tribromides, and Triiodides of Americium and Curium, in: Inorg. Chem., 1965, 4 (7), S. 985–986 (doi:10.1021/ic50029a013).
- ↑ John H. Burns, Joseph Richard Peterson: The Crystal Structures of Americium Trichloride Hexahydrate and Berkelium Trichloride Hexahydrate, in: Inorg. Chem., 1971, 10 (1), S. 147–151 (doi:10.1021/ic50095a029).
- ↑ OECD Nuclear Energy Agency: Proceedings of the Workshop on Pyrochemical Separations. Nuclear Energy Agency, Organisation for Economic Co-operation and Development, 2001, ISBN 978-92-64-18443-5, S. 276–277 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ DIANE Publishing: Plutonium Processing In The Nuclear Weapons Complex. DIANE Publishing, 1992, ISBN 978-1-56806-568-7, S. 21 (eingeschränkte Vorschau in der Google-Buchsuche).
Literatur
- Wolfgang H. Runde, Wallace W. Schulz: Americium, in: Lester R. Morss, Norman M. Edelstein, Jean Fuger (Hrsg.): The Chemistry of the Actinide and Transactinide Elements, Springer, Dordrecht 2006; ISBN 1-4020-3555-1, S. 1265–1395 (doi:10.1007/1-4020-3598-5_8).