2-Iodosylbenzoesäure
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
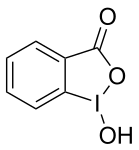
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 2-Iodosylbenzoesäure | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C7H5IO3 | ||||||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 263,93 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
2-Iodosylbenzoesäure (kurz: IBA nach engl. iodosylbenzoic acid) ist eine chemische Verbindung aus der Gruppe der hypervalenten Iodverbindungen. Es entsteht als Abfallprodukt bei der IBX-Oxidation.[3]
Gewinnung und Darstellung
2-Iodosylbenzoesäure wurde erstmals 1892 von Victor Meyer und Wilhelm Wachter durch kurzes Kochen von 2-Iodbenzoesäure in rauchender Salpetersäure, Ausfällen und Umkristallisieren aus Wasser hergestellt.[4]
Eigenschaften
Physikalische Eigenschaften
2-Iodosylbenzoesäure verpufft bei schneller Erhitzung.[4]
Chemische Eigenschaften
2-Iodosylbenzoesäure oxidiert Kaliumiodid in Lösung zu elementarem Iod, wird dabei selbst zu Kaliumacetat und 2-Iodbenzoesäure reduziert. Auch Chlorwasserstoff wird derartig oxidiert. Mit elementarem Zink in ammoniakalischer Lösung reagiert 2-Iodosylsäure zu Benzoesäure. Aufgrund des schwach sauren Charakters löst sich 2-Iodosylbenzoesäure in basischer wässriger Lösung und wird durch Säuren wieder ausgefällt.[4]
Nachweis
2-Iodosylbenzoesäure kann durch Iodometrie mit Natriumthiosulfat bestimmt werden.[4]
Einzelnachweise
- ↑ a b c d Datenblatt 1-Hydroxy-3-oxo-1,3-dihydro-1,2-benzoiodoxole (PDF) bei BLD Pharmatech, Katalognummer: BD210508 , abgerufen am 26. August 2025.
- ↑ Yao-Feng Wang, Jiashen Qiu, Dejie Kong, Yongtao Gao, Feipeng Lu, Pran Gopal Karmaker, Fu-Xue Chen: The direct electrophilic cyanation of β-keto esters and amides with cyano benziodoxole. In: Organic & Biomolecular Chemistry. Band 13, Nr. 2, 2015, S. 365–368, doi:10.1039/C4OB02032D.
- ↑ Supanimit Chiampanichayakul, Manat Pohmakotr, Vichai Reutrakul, Thaworn Jaipetch, Chutima Kuhakarn: Oxidative Conversion of Amines into Their Corresponding Nitriles Using o -Iodoxybenzoic Acid (IBX)/Iodine: Selective Oxidation of Aminoalcohols to Hydroxynitriles. In: Synthesis. Band 2008, Nr. 13, 11. Juni 2008, S. 2045–2048, doi:10.1055/s-2008-1067123.
- ↑ a b c d Victor Meyer, Wilhelm Wachter: Ueber Jodosobenzoësäure. In: Berichte der deutschen chemischen Gesellschaft. Band 25, Nr. 2, Juli 1892, S. 2632–2635, doi:10.1002/cber.18920250280.

