1-Methylnicotinamid
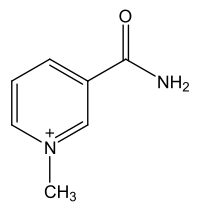
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||
| Kation, Anion (meist Halogenid, wie Chlorid oder Iodid) nicht abgebildet | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | 1-Methylnicotinamid | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel |
| |||||||||||||||
| Kurzbeschreibung |
weißes Pulver[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | ||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
leicht in Wasser (15 mg·ml−1 bei 20 °C)[1] (Chlorid) | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
1-Methylnicotinamid (1-MNA) ist das methylierte Amid der Nicotinsäure (Niacin, Vitamin B3). Es ist eine körpereigene Substanz, die in der Leber bei der Verstoffwechselung von Nicotinamid hergestellt wird. Es ist am sogenannten Nikotinamid-Rückgewinnungsweg im NAD+ (Nikotinamid-Adenin-Dinukleotid)-Stoffwechselweg beteiligt und trägt somit zur Optimierung des NAD+-Spiegels bei.[5]
Vorkommen
Die höchste natürliche Konzentration von 1-Methylnicotinamid (1-MNA) ist in der Alge Undaria pinnatifida (3,2 mg/100 g Trockenalgen) und Grünteeblättern (3 mg/100 g Produkt) zu finden.[6] Weitere Produkte mit den höchsten natürlichen Konzentrationen an 1-MNA sind Sellerie (1,6 mg/100 g Produkt), chinesische schwarze Pilze, die sogenannten Shiitake (1,3 mg/100 g Pilze) und fermentiertes Soja, das sogenannte Natto (1,0 mg/100 g Produkt).[6]
Biosynthese
1-Methylnicotinamid wird primär in der Leber durch die Nicotinamid-N-Methyltransferase hergestellt. Die Reaktion findet im Laufe der Verstoffwechselung von NAD+ (Nicotinamidadenindinukleotid) statt. NNMT findt sich auch im Hirngewebe, Fettgewebe, Muskelgewebe, in den Nieren und in der Haut.[7][8]
Die Rolle im Organismus
Wissenschaftliche Untersuchungen belegen zahlreiche therapeutische und gesundheitsfördernde Eigenschaften von 1-MNA, darunter gefäßschützende[9][10], anti-koagulatorische[11], anti-atherosklerotische[12], entzündungshemmende[13][14][15], neuroprotektive[16] und die Funktionsfähigkeit des Organismus steigernde Effekte.[17]
Gefäßschützende Wirkung
1-Methylnicotinamid hat durch seine Wirkung auf das Gefäßendothel eine positive Wirkung auf die Blutgefäße. Es verbessert die Bioverfügbarkeit von Stickstoffmonoxid (NO), das für die Gefäßerweiterung entscheidend ist, und reguliert die Aktivität der endothelialen Nitritoxidsynthase (eNOS), des für die NO-Synthese zuständigen Enzyms.[9][10]
Diese Wirkung ist in In-vivo- und In-vitro-Studien nachgewiesen worden. Oral an gesunde und hypercholesterinämische Personen verabreicht, erhöht 1-MNA den Durchmesser der Arteria brachialis (FMD-Messung) und stimuliert die Sekretion von Stickstoffmonoxid (NO) durch die menschlichen Endothelzellen.[10]
Darüber hinaus stellte 1-MNA die normale Stickstoffmonoxid (NO)-abhängige Vasodilatation bei gestörter Gefäßfunktion (Hypertriglyceridämie oder Diabetes) wieder her.[9]
1-MNA kann durch die Erhöhung der NO-Bioverfügbarkeit einer endothelialen Dysfunktion entgegenwirken, die endotheliale Regeneration fördern und die Gefäßfunktion bei kardiovaskulärem Risiko verbessern.[9][10]
Anti-koagulatorische Wirkung
1-Methylnicotinamid ist ein endogener Aktivator der Prostacyclin-Synthese und kann daher trombolytische und entzündliche Prozesse im kardiovaskulären System regulieren. Es hemmt die plättchenabhängige Thrombose durch einen Mechanismus, an dem Cyclooxygenase-2 und Prostacyclin (PGI2) beteiligt sind[11] und erhöht die Stickoxid-Bioverfügbarkeit im Endothel.[10] Das körpereigene Prostazyklin (PGI2) ist unter anderem für die anti-thrombotische und anti-atherosklerotische Wirkung verantwortlich. Sein Mangel verursacht eine erhöhte Thrombozytenaggregation und Gerinnselbildung in den Arterien.
Anti-atherosklerotische und entzündungshemmende Wirkung
1-MNA weist eine anti-atherosklerotische und entzündungshemmende Wirkung auf. Sie wird mit einer verbesserten Prostazyklin- und Stickoxid-abhängigen vaskulären endothelialen Sekretionsfunktion, einer Hemmung der Thrombozytenaktivierung, einer Verringerung der Entzündung in der atherosklerotischen Plaque, einer Hemmung der systemischen Entzündung und einer Verringerung der TNF-α-Spiegel in Verbindung gebracht.[12]
Die in mehreren Studien nachgewiesene entzündungshemmende Wirkung von 1-MNA ist auf seine Fähigkeit zurückzuführen, die Sekretion von körpereigenem PGI2 zu stimulieren, sowie auf seine Wirkung, die IL-4 und TNF-α-Spiegel zu senken.[13] Die entzündungshemmende Wirkung von 1-MNA hängt mit endothelialen Mechanismen zusammen und nicht mit einer direkten Wirkung auf die Funktion der Immunzellen, sodass sie die Reaktion des Körpers nicht beeinträchtigt.[14][15]
NAD+-Optimierung
1-Methylnicotinamid ist ein Inhibitor der Nicotinamid-N-Methyltransferase (NNMT). Durch die Hemmung der NNMT-Aktivität beeinflusst es die Regulierung der NAD+ (Nicotinamid-Adenin-Dinukleotid)-Biosynthese über den sogenannten Nicotinamid-Rückgewinnungsweg, den Hauptweg der NAD+-Synthese bei Säugetieren. 1-MNA, das am Nikotinamid-Rückgewinnungsweg beteiligt ist, optimiert den NAD+-Spiegel.[5]
Auswirkungen auf SIRT1
Literaturberichte, die im Nature Medicine veröffentlicht wurden, weisen darauf hin, dass 1-MNA die Expression von SIRT1 erhöht und dessen Stabilisierung beeinflusst. SIRT1 ist ein Enzym, das mit Langlebigkeit in Verbindung gebracht wird.[18] Versuche mit dem Fadenwurm Caenorhabditis elegans zeigten, das bei Zugabe von 1-Methylnicotinamid ihre Lebensdauer verlängert werden kann.[19]
Neuroprotektive Wirkungen
Tierversuche an Ratten mit Diabetes haben gezeigt, dass sich 1-Methylnicotinamid positiv auf degenerative Veränderungen im Gehirn auswirkt, sodass die kognitiven Leistungen länger aufrechterhalten werden können.[20]
1-MNA beugt depressivem Verhalten vor, indem es eine vergleichbare Wirksamkeit wie ein gängiges Antidepressivum (Fluoxetin) erzielt. Diese Wirkung von 1-MNA ist wahrscheinlich auf eine Verringerung der im depressiven Zustand auftretenden Neuroinflammation, eine Verringerung der pro-inflammatorischen Zytokine (IL-6, TNF-α) und eine Erhöhung der Expression des BDNF-Proteins (brain-derived neurotrophic factor, ein Protein, das das Überleben bestehender Neuronen unterstützt und das Wachstum und die Differenzierung neuer Neuronen und Synapsen stimuliert) zurückzuführen.[21]
Die neuroprotektive Wirkung von 1-Methylnicotinamid ist auf seine Fähigkeit zurückzuführen, vor bestimmten Neurotoxinen, vor den toxischen Auswirkungen der im Gehirn abgelagerten Peptidplaques (Aβ), seiner hemmenden Wirkung auf die neuroinflammatorische Reaktion und die Apoptose von Nervenzellen zu schützen. 1-MNA hat eine positive Wirkung auf die Verbesserung von Gedächtnisdefiziten und kognitiven Funktionen.[16] 1-MNA könnte eine neue Strategie für Gedächtnis-, Lern- und andere neurodegenerative Erkrankungen sein.[22][16]
Auswirkungen auf die Leistungsfähigkeit des Organismus
1-Methylnicotinamid wirkt als Myokin, das dem Körper hilft, Aminosäuren für die Gluconeogenese in der Leber zu verwenden und die Lipolyse im Fettgewebe zu stimulieren, die den Muskeln Energie liefert.[23] Studien zeigen, dass die Einnahme von 1-MNA die körperliche Belastbarkeit verbessert und die Müdigkeit verringert. Nach einem Monat der Einnahme von 1-MNA berichteten die COVID-19-Patienten über eine Verbesserung der beim 6-Minuten-Gehtest (6MWT) erzielten Distanz. 92 % der Anwender von 1-MNA berichteten über eine Verbesserung der Testergebnisse, und viele berichteten auch über weniger Müdigkeit. Die Verbesserung der Distanz war bei 1-MNA-Anwendern dreimal so hoch wie in der Kontrollgruppe.[17]
Nachfolgende Studien weisen erneut auf die Fähigkeit von 1-MNA hin, die körperliche Leistungsfähigkeit zu verbessern. Diese Wirkung steht im Zusammenhang mit der Stimulierung der PGI2-Freisetzung, die die koronare, pulmonale und periphere Mikrozirkulation vor der Bildung von Thrombozyten-Mikroaggregaten schützt und die angemessene Blutversorgung des Muskelgewebes beeinflusst. Durch diesen Mechanismus kann 1-MNA vor dem durch körperliche Anstrengung ausgelösten kardiovaskulären Risiko schützen, insbesondere bei einer gestörten vaskulären Endothelfunktion.[24]
Kommerzialisierung
1-Methylnicotinamid ist für die Verwendung in Lebensmitteln in Form von 1-Methylnicotinamidchlorid zugelassen.
Das Verfahren zur Meldung und Registrierung von 1-MNA-Chlorid als neuartiges Lebensmittel in der Europäischen Union wurde von der PHARMENA SA erfolgreich durchgeführt. Im Jahr 2017 wurde ein Gutachten der Europäischen Behörde für Lebensmittelsicherheit (EFSA) veröffentlicht, das die Sicherheit von 1-MNA-Chlorid in Lebensmitteln (Nahrungsergänzungsmitteln) bestätigt.[25] Auf der Grundlage eines positiven Gutachtens der EFSA im Jahr 2018 hat die Europäische Kommission 1-MNA-Chlorid mit der Durchführungsverordnung 2018/1123 als neuartiges Lebensmittel im Segment der Nahrungsergänzungsmittel zugelassen und der PHARMENA SA das Recht eingeräumt, die Antragsdaten zu schützen.[26]
Sicherheit
Die Sicherheit von 1-MNA-Chlorid wurde von der Europäischen Behörde für Lebensmittelsicherheit (EFSA) eingehend bewertet. Eine wissenschaftliche Bewertung hat gezeigt, dass 1-MNA sicher in der Anwendung ist.[25]
Das in Lebensmitteln verfügbare 1-MNA-Chlorid muss den Qualitätsparametern entsprechen, die in der Durchführungsverordnung (EU) 2018/1123 der Kommission festgelegt sind.[26]
Einzelnachweise
- ↑ a b c d e Datenblatt 1-Methylnicotinamide Chloride bei Sigma-Aldrich, abgerufen am 29. Januar 2020 (PDF).
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu 3-Carbamoyl-1-methylpyridiniumchlorid: CAS-Nr.: 1005-24-9, EG-Nr.: 463-670-7, ECHA-InfoCard: 100.104.777, PubChem: 70495, ChemSpider: 63668, Wikidata: Q27282725.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu 3-Carbamoyl-1-methylpyridiniumiodid: CAS-Nr.: 6456-44-6, EG-Nr.: 229-263-1, ECHA-InfoCard: 100.026.603, PubChem: 72660, ChemSpider: 65521, Wikidata: Q82970083.
- ↑ Kosower, E. M.; Klinedinst, P. E.: "Additions of pyridinium rings. II. Charge-transfer complexes as intermediates" in J. Am. Chem. Soc. 78 (1956) 3493–3497.
- ↑ a b Jing-Jing Li, Wei-Dong Sun, Xiao-Juan Zhu, Ya-Zhong Mei, Wen-Song Li, Jiang-Hua Li: Nicotinamide N-Methyltransferase (NNMT): A New Hope for Treating Aging and Age-Related Conditions. In: Metabolites. Band 14, Nr. 6, 19. Juni 2024, S. 343, doi:10.3390/metabo14060343, PMID 38921477, PMC 11205546 (freier Volltext).
- ↑ a b Taguchi, H.; Sakaguchi, M.; Shimbabayashi, Y.: "Contents of quinolinic acid trigonelline and N-1 methylnicotinamide in various foods and thermal conversion of these compounds into nicotinic acid and nicotinamide" in [Vitamins] 60 (1986) 537–546.
- ↑ GTEx Portal. Abgerufen am 14. Januar 2025.
- ↑ BioGPS - your Gene Portal System. Archiviert vom am 5. Januar 2025; abgerufen am 14. Januar 2025 (englisch).
- ↑ a b c d Bartus, M.; Lomnicka, M.; Kostogrys, R. B.; Kazmierczak, P.; Watala, C.; Slominska, E.M.; Smolenski, R.T.; Pisulewski, P.M.; Adamus, J.; Gebicki, J.; Chlopicki, S.: "1-Methylnicotinamide (MNA) prevents endothelial dysfunction in hypertriglyceridemic and diabetic rats" in Pharmacol. Rep. 60 (2008) 127–138.
- ↑ a b c d e Domagala, T. B.; Szeffler, A.; Dobrucki, L. W.; Dropinski, J.; Polanski, S.; Leszczynska-Wiloch, M.; Kotula-Horowitz, K.; Wojciechowski, J.; Wojnowski, L.; Szczeklik, A.; Kalinowski, L.: "Nitric oxide production and endothelium-dependent vasorelaxation ameliorated by N1-methylnicotinamide in human blood vessels" in Hypertension 59 (2012) 825–832.
- ↑ a b Chlopicki, S.; Swies, J.; Mogielnicki, A.; Buczko, W.; Bartus, M.; Lomnicka, M.; Adamus, J.; Gebicki, J.: "1-Methylnicotinamide (MNA), a primary metabolite of nicotinamide, exerts anti-thrombotic activity mediated by a cyclooxygenase-2/prostacyclin pathway" in Br. J. Pharmacol. 152 (2007) 230–239.
- ↑ a b L. Mateuszuk, A. Jasztal, E. Maslak, M. Gasior-Glogowska, M. Baranska, B. Sitek, R. Kostogrys, A. Zakrzewska, A. Kij, M. Walczak, S. Chlopicki: Antiatherosclerotic Effects of 1-Methylnicotinamide in Apolipoprotein E/Low-Density Lipoprotein Receptor-Deficient Mice: A Comparison with Nicotinic Acid. In: Journal of Pharmacology and Experimental Therapeutics. Band 356, Nr. 2, 22. Januar 2016, S. 514–524, doi:10.1124/jpet.115.228643, PMID 26631491, PMC 6047228 (freier Volltext).
- ↑ a b Andrzej Jakubowski, Magdalena Sternak, Konrad Jablonski, Marta Ciszek-Lenda, Janusz Marcinkiewicz, Stefan Chlopicki: 1-Methylnicotinamide protects against liver injury induced by concanavalin A via a prostacyclin-dependent mechanism: A possible involvement of IL-4 and TNF-α. In: International Immunopharmacology. Band 31, Februar 2016, S. 98–104, doi:10.1016/j.intimp.2015.11.032.
- ↑ a b Bryniarski, K.; Biedron, R.; Jakubowski, A.; Chlopicki, S.; Marcinkiewicz, J.: "Anti-inflammatory effect of 1-methylnicotinamide in contact hypersensitivity to oxazolone in mice; involvement of prostacyclin" in Eur. J. Pharmacol. 578 (2008) 332–338.
- ↑ a b Rafał Biedroń, Marta Ciszek, Marianna Tokarczyk, Małgorzata Bobek, Maria Kurnyta, Ewa M. Słominska, Ryszard T. Smoleński, Janusz Marcinkiewicz: 1-Methylnicotinamide and nicotinamide: two related anti-inflammatory agents that differentially affect the functions of activated macrophages. In: Archivum Immunologiae et Therapiae Experimentalis. Band 56, Nr. 2, April 2008, S. 127–134, doi:10.1007/s00005-008-0009-2, PMID 18373238, PMC 2766500 (freier Volltext).
- ↑ a b c Lili Fu, Caihong Liu, Liang Chen, Yangge Lv, Guoliang Meng, Mei Hu, Yan Long, Hao Hong, Susu Tang: Protective Effects of 1-Methylnicotinamide on Aβ1–42-Induced Cognitive Deficits, Neuroinflammation and Apoptosis in Mice. In: Journal of Neuroimmune Pharmacology. Band 14, Nr. 3, September 2019, S. 401–412, doi:10.1007/s11481-018-09830-1.
- ↑ a b Michał Chudzik, Monika Burzyńska, Joanna Kapusta: Use of 1-MNA to Improve Exercise Tolerance and Fatigue in Patients after COVID-19. In: Nutrients. Band 14, Nr. 15, 22. Juli 2022, S. 3004, doi:10.3390/nu14153004, PMID 35893858, PMC 9331270 (freier Volltext).
- ↑ Shangyu Hong, Jose M Moreno-Navarrete, Xiaojing Wei, Yusuke Kikukawa, Iphigenia Tzameli, Deepthi Prasad, Yoonjin Lee, John M Asara, Jose Manuel Fernandez-Real, Eleftheria Maratos-Flier, Pavlos Pissios: Nicotinamide N-methyltransferase regulates hepatic nutrient metabolism through Sirt1 protein stabilization. In: Nature Medicine. Band 21, Nr. 8, August 2015, S. 887–894, doi:10.1038/nm.3882, PMID 26168293, PMC 4529375 (freier Volltext).
- ↑ Schmeisser, K.; Mansfeld, J.; Kuhlow, D.; Weimer, S.; Priebe, S.; Heiland, I.; Birringer, M.; Groth, M.; Segref, A.; Kanfi, Y.: "Role of Sirtuins in Lifespan Regulation is Linked to Methylation of Nicotinamide" in Nat. Chem. Biol. 9 (2013) 693–700.
- ↑ Tamara Kuchmerovska, Ihor Shymanskyy, Stefan Chlopicki, Arkady Klimenko: 1-Methylnicotinamide (MNA) in prevention of diabetes-associated brain disorders. In: Neurochemistry International. Band 56, Nr. 2, Januar 2010, S. 221–228, doi:10.1016/j.neuint.2009.10.004.
- ↑ Jie Zhao, Yin Zhang, Yue Liu, Wen-Qian Tang, Chun-Hui Ji, Jiang-Hong Gu, Bo Jiang: Antidepressant-like effects of 1-methylnicotinamide in a chronic unpredictable mild stress model of depression. In: Neuroscience Letters. Band 742, Januar 2021, S. 135535, doi:10.1016/j.neulet.2020.135535.
- ↑ Zeinab H. Milani, David B. Ramsden, Richard B. Parsons: Neuroprotective Effects of Nicotinamide N ‐Methyltransferase and its Metabolite 1‐Methylnicotinamide. In: Journal of Biochemical and Molecular Toxicology. Band 27, Nr. 9, September 2013, S. 451–456, doi:10.1002/jbt.21508.
- ↑ Hamid Reza Nejabati, Mahsa Ghaffari-Novin, Nazila Fathi-Maroufi, Yousef Faridvand, Hans-Christer Holmberg, Ola Hansson, Saba Nikanfar, Mohammad Nouri: N1-Methylnicotinamide: Is it Time to Consider it as a Dietary Supplement for Athletes? In: Current Pharmaceutical Design. Band 28, Nr. 10, März 2022, S. 800–805, doi:10.2174/1381612828666220211151204.
- ↑ Kamil Przyborowski, Marta Wojewoda, Barbara Sitek, Agnieszka Zakrzewska, Agnieszka Kij, Krystyna Wandzel, Jerzy Andrzej Zoladz, Stefan Chlopicki: Effects of 1-Methylnicotinamide (MNA) on Exercise Capacity and Endothelial Response in Diabetic Mice. In: PLOS ONE. Band 10, Nr. 6, 26. Juni 2015, S. e0130908, doi:10.1371/journal.pone.0130908, PMID 26115505, PMC 4482656 (freier Volltext).
- ↑ a b EFSA Panel on Dietetic Products, Nutrition and Allergies (NDA), Dominique Turck, Jean‐Louis Bresson, Barbara Burlingame, Tara Dean, Susan Fairweather‐Tait, Marina Heinonen, Karen Ildico Hirsch‐Ernst, Inge Mangelsdorf, Harry J McArdle, Androniki Naska, Monika Neuhäuser‐Berthold, Grażyna Nowicka, Kristina Pentieva, Yolanda Sanz, Alfonso Siani, Anders Sjödin, Martin Stern, Daniel Tomé, Marco Vinceti, Peter Willatts, Karl‐Heinz Engel, Rosangela Marchelli, Annette Pöting, Morten Poulsen, Josef Rudolf Schlatter, Wolfgang Gelbmann, Ermolaos Ververis, Henk van Loveren: Safety of 1‐methylnicotinamide chloride (1‐MNA) as a novel food pursuant to Regulation (EC) No 258/97. In: EFSA Journal. Band 15, Nr. 10, Oktober 2017, doi:10.2903/j.efsa.2017.5001, PMID 32625296, PMC 7010160 (freier Volltext).
- ↑ a b Implementing regulation - 2018/1123 - EN - EUR-Lex. Abgerufen am 15. Januar 2025 (englisch).