1,1,1,2-Tetrachlorethan
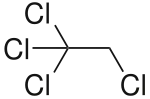
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 1,1,1,2-Tetrachlorethan | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C2H2Cl4 | ||||||||||||||||||
| Kurzbeschreibung |
flüchtige, farblose Flüssigkeit[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 167,85 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Dichte |
1,6 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
138 °C[1] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit |
schwer in Wasser (1,07 g·l−1 bei 25 °C)[1] | ||||||||||||||||||
| Brechungsindex |
1,481 (20 °C)[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
1,1,1,2-Tetrachlorethan ist eine chemische Verbindung aus der Gruppe der aliphatischen gesättigten Halogenkohlenwasserstoffe und organischen Chlorverbindungen. Sie ist isomer zu 1,1,2,2-Tetrachlorethan.
Gewinnung und Darstellung
1,1,1,2-Tetrachlorethan kann durch zweistufige Additionsreaktion von Ethin mit Chlor (über Dichlorethen) gewonnen werden, wobei jedoch hauptsächlich 1,1,2,2-Tetrachlorethan entsteht.
Es kann direkt durch Chlorierung von 1,1,2-Trichlorethan gewonnen werden.[3]
Es tritt auch als Verunreinigung bei der Herstellung von einigen weit verbreiteten chlorierten Kohlenwasserstoffen auf.[4]
Eigenschaften
1,1,1,2-Tetrachlorethan ist ein brennbare, flüchtige, farblose Flüssigkeit, welche wenig löslich in Wasser ist.[1] Bei 500–600 °C pyrolysiert es, wobei unter anderem Trichlorethen und Chlorwasserstoff entstehen. Durch Disproportionierung entsteht auch Tetrachlorethen.[5] Ein weiteres Nebenprodukt ist Hexachlorbenzol, welches durch Polymerisation von Dichloracetylen entsteht.[6]
Verwendung
Es wird als Lösungsmittel und zur Herstellung von Lasuren und Lacken sowie als Zwischenprodukt zur Herstellung von Trichlorethen und Tetrachlorethen verwendet. In den USA ist es in geringen Konzentrationen auch in der Luft und im Trinkwasser nachgewiesen worden.[4]
Sicherheitshinweise
Die IARC stufte 1,1,1,2-Tetrachlorethan im Jahr 2014 als möglicherweise krebserzeugend ein.[7]
Literatur
- E. N. Culubret, M. Luz, R. Amils, J. L. Sanz: Biodegradation of 1,1,1,2-tetrachloroethane under methanogenic conditions. In: Water Science and Technology: A Journal of the International Association on Water Pollution Research. Band 44, Nr. 4, 2001, S. 117–122, PMID 11575074.
Weblinks
Einzelnachweise
- ↑ a b c d e f g h i j Eintrag zu 1,1,1,2-Tetrachlorethan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 10. Januar 2025. (JavaScript erforderlich)
- ↑ Datenblatt 1,1,1,2-Tetrachlorethan bei Sigma-Aldrich, abgerufen am 5. März 2011 (PDF).
- ↑ Lawrance Waddams: The Petroleum chemicals Industry, S. 175.
- ↑ a b IARC Working Group on the Evaluation of Carcinogenic Risks to Humans (Hrsg.): Re-evaluation of some organic chemicals, hydrazine and hydrogen peroxide (= IARC monographs on the evaluation of carcinogenic risks to humans. Band 71). World Health Organization, International Agency for Research on Cancer, Lyon, France 1999, ISBN 978-92-832-1271-3 (iarc.fr).
- ↑ Eberhard-Ludwig Dreher, Klaus K. Beutel, John D. Myers, Thomas Lübbe, Shannon Krieger, Lynn H. Pottenger: Ullmann's Encyclopedia of Industrial Chemistry. John Wiley & Sons, Ltd, 2014, Chloroethanes and Chloroethylenes, S. 1–81, doi:10.1002/14356007.o06_o01.pub2.
- ↑ D. H. R. Barton, K. E. Howlett: 451. The kinetics of the dehydrochlorination of substituted hydrocarbons. Part VII. The mechanism of the thermal decompositions of 1:1:2:2- and 1:1:1:2-tetrachloroethane. In: Journal of the Chemical Society (Resumed). Nr. 0, 1951, S. 2033–2038, doi:10.1039/JR9510002033.
- ↑ IARC Working Group on the Evaluation of Carcinogenic Risks to Humans (Hrsg.): Trichloroethylene, tetrachloroethylene, and some other chlorinated agents (= IARC monographs on the evaluation of carcinogenic risks to humans. Band 106). International Agency for Research on Cancer, Lyon 2014, ISBN 978-92-832-0144-1 (iarc.fr).


